抗血小板药物(APAs)通过抑制血小板的聚集和活化以预防和减少血栓形成,是治疗血栓的关键药物之一。但是APAs使用过量容易导致严重出血,如颅内出血、消化道出血和脏器出血等,从而给患者带来生命危险,因而该类药物在临床上使用的剂量范围较窄,因使用风险很高而受到限制。但是,如果在患者使用APAs而导致出血或紧急侵入性手术前,及时清除过量的APAs,或采取相应的逆转策略使血小板恢复止血功能,将减轻APAs的副作用,提高其临床使用的安全性。然而目前市场上还没有相关的逆转剂被研发出来。
针对上述问题,国家纳米中心张银龙教授团队与我院刘继华教授课题组联合开发了以点击化学修饰的金纳米颗粒AuNPs-PEG-DBCO和AuNPs-PEG-MAL,能够分别减轻抗血小板药物N3-替格瑞洛和氯吡格雷引起的出血现象,促进血小板功能的恢复,从而逆转N3-替格瑞洛和氯吡格雷药物的抗血小板作用,提高药物使用的安全性。
研究中依据含有二苯并环辛炔(DBCO)配体的小分子能够与含有叠氮基团的APAs结合的特性,合成了金纳米颗粒AuNPs-PEG-DBCO,在体内能够与N3-替格瑞洛快速结合,从而逆转其抗血小板作用;而含有马来酰亚胺(MAL)配体的小分子能够与含有巯基的APAs活性代谢物结合,将其修饰到金纳米颗粒上,合成出AuNPs-PEG-MAL,能够与氯吡格雷活性代谢产物(CLP-AM)快速结合,从而起到功能逆转的作用。体外结合实验证实,AuNPs-PEG-DBCO与N3-替格瑞洛的结合效率为88.0±3.43%,AuNPs-PEG-MAL与CLP-AM的结合效率为45.45±6.89%。表明功能化的纳米颗粒可以在室温条件下与抗血小板药物结合。体内尾尖出血模型实验表明,AuNPs-PEG-DBCO和AuNPs-PEG-MAL可显著缩短N3-替格瑞洛和氯吡格雷尾尖出血时间,在最长出血时间点的逆转效率分别为43.85%和64.31%;体内急性肝损伤小鼠模型实验同样表明AuNPs-PEGDBCO和AuNPs-PEG-MAL对N3-替格瑞洛和CLP-AM的逆转效率分别为68.53%和62.12%,均高于血小板输注的逆转效率19.73%和28.25%。综上所述,体外和体内实验均证明,AuNPs-PEG-DBCO和AuNPs-PEG-MAL 能够促进血小板功能的恢复,并减轻N3-替格瑞洛和氯吡格雷引起的出血现象。本研究提出了利用点击化学修饰的金纳米颗粒去逆转APAs抗血小板功能的新策略,有望通过控制出血风险来提高临床上APAs的用药安全性,同时为AuNPs的临床应用转化,构建诊断、治疗和预防一体化平台提供了新的方向和思路。
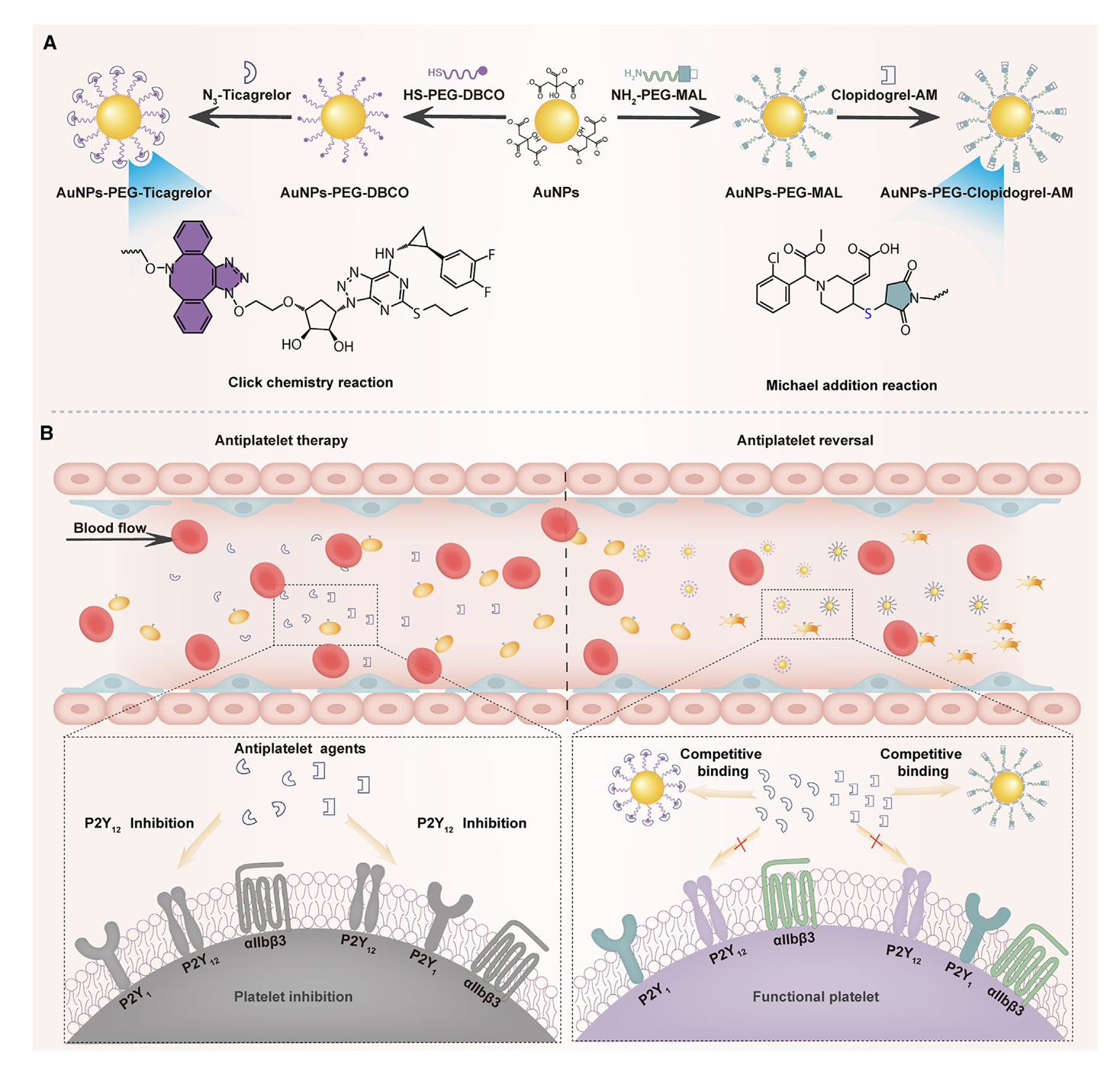
图1. 点击化学修饰金纳米颗粒的设计特点和作用机理
(a) AuNPs-PEG-DBCO和AuNPs-PEG-MAL的合成和与药物结合示意图。(b)点击化学修饰的金纳米颗粒的工作机制示意图。
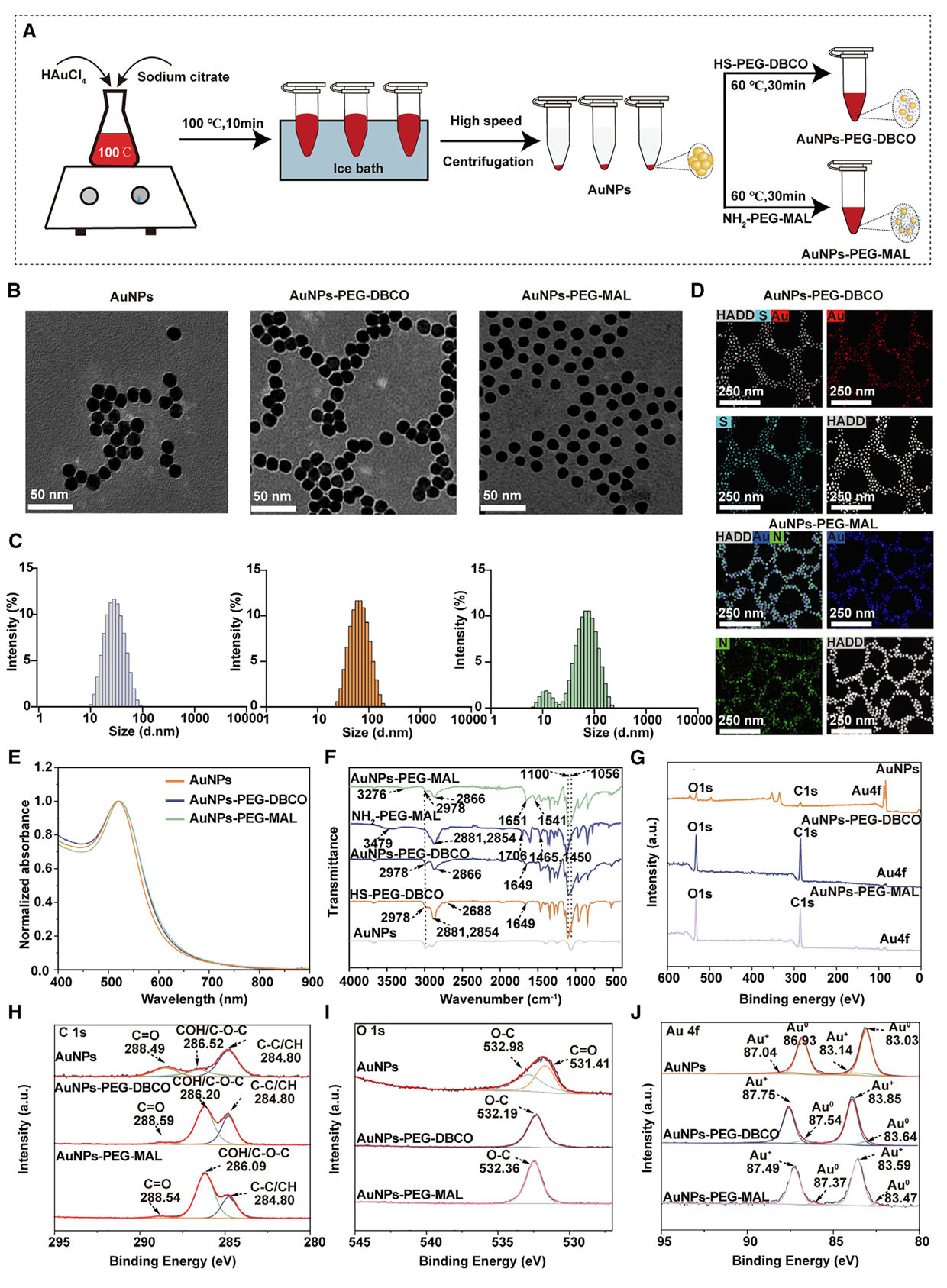
图2. 金纳米颗粒和功能化金纳米颗粒的物理化学表征
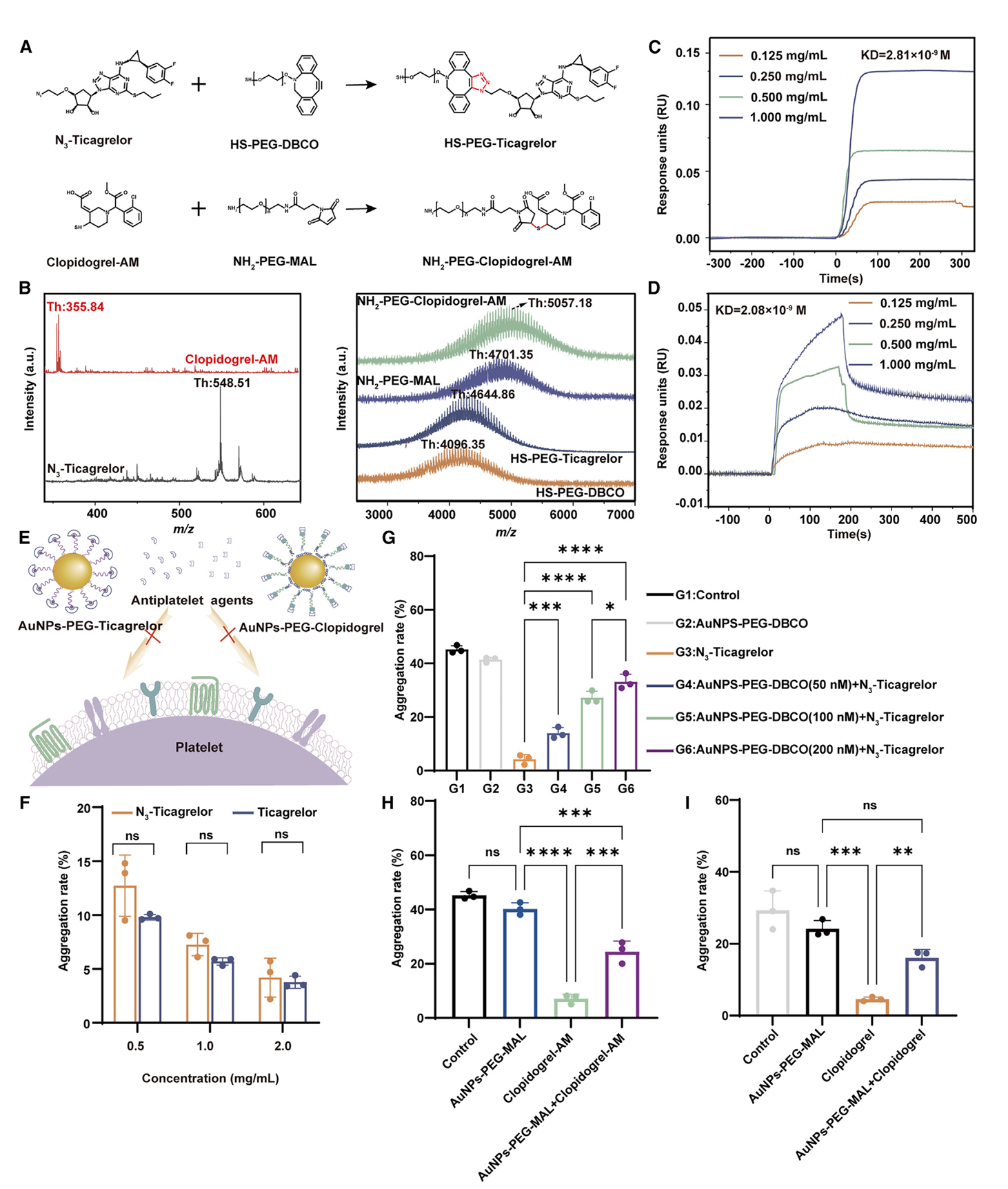
图3. AuNPs-PEG-DBCO和AuNPs-PEG MAL与APAs的结合和抗血小板功能逆转作用
(a) HS-PEG-DBCO和NH2-PEG-MAL分别与N3替格瑞洛和氯吡格雷的活性代谢产物发生化学反应;(b)N3替格瑞洛、氯吡格雷AM、HS-PEG-DBCO和N3替格瑞洛的结合物、NH2-PEG-MAL和氯吡格雷AM的结合物的基质辅助激光解吸电离飞行时间质谱(MALDI-TOF-MS);(c)SPR法测定HS-PEG-DBCO与N3替格瑞洛的结合亲和力;(d)NH2-PEG-MAL和氯吡格雷AM的结合亲和力;(e)血小板聚集率试验示意图。(f)氯吡格雷和N3替格瑞洛在血小板聚集试验中的抗血小板活性(n=3)。(g)在血小板聚集试验中,AuNPs-PEG-DBCO对N3-Ticagrelor的体外功能逆转(n=3)。(h)在血小板聚集试验中,AuNPs-PEG-MAL对氯吡格雷AM的体外功能逆转(n=3)。(i)AuNPs-PEG-MAL在血小板聚集试验中逆转氯吡格雷的体外功能(n=3)。*P<0.05;**P<0.01;***P<0.001;****P<0.0001
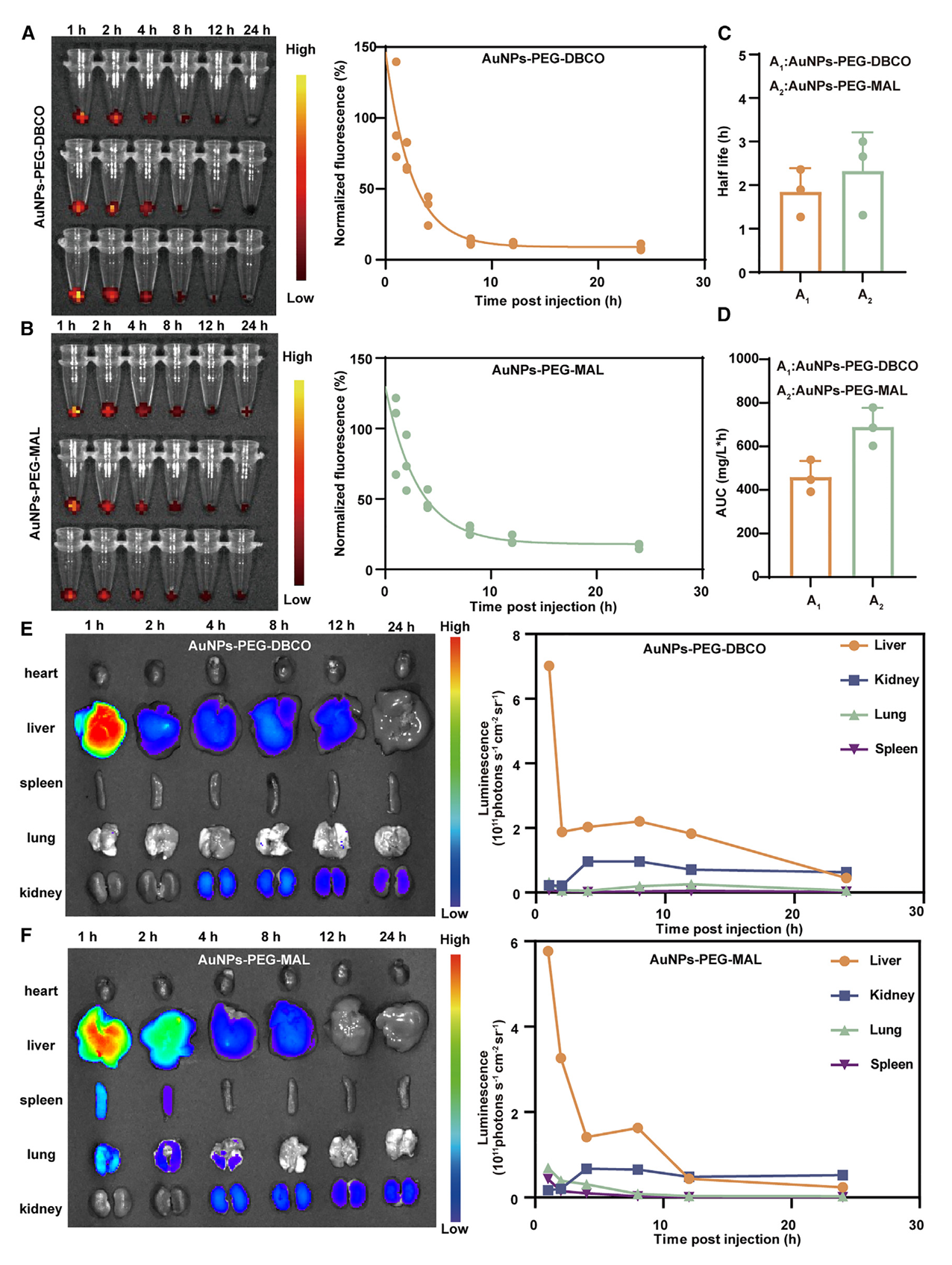
图4. AuNPs-PEG-DBCO和AuNPs-PEG-MAL的药代动力学和生物分布
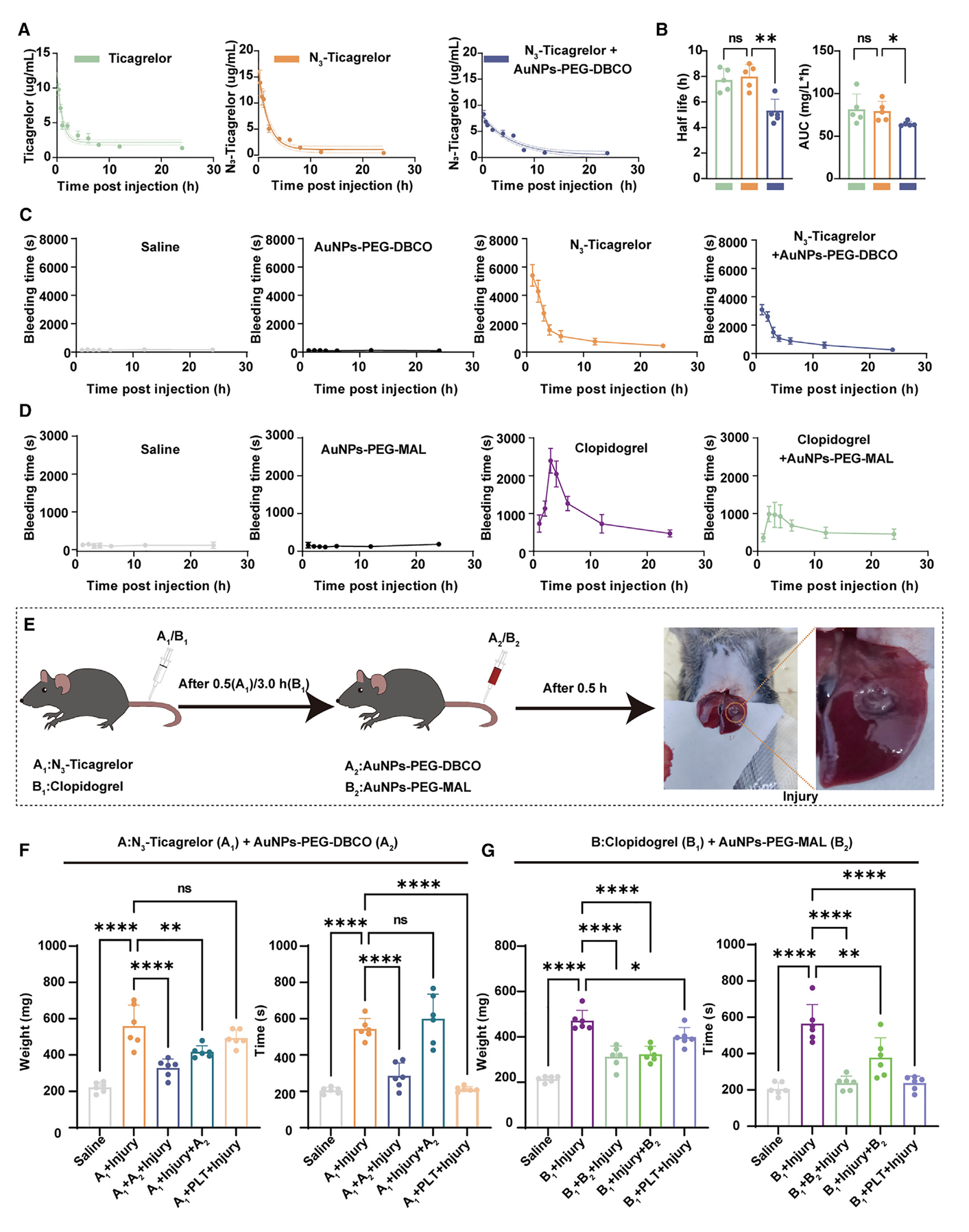
图5:APAs的体内消除和功能逆转
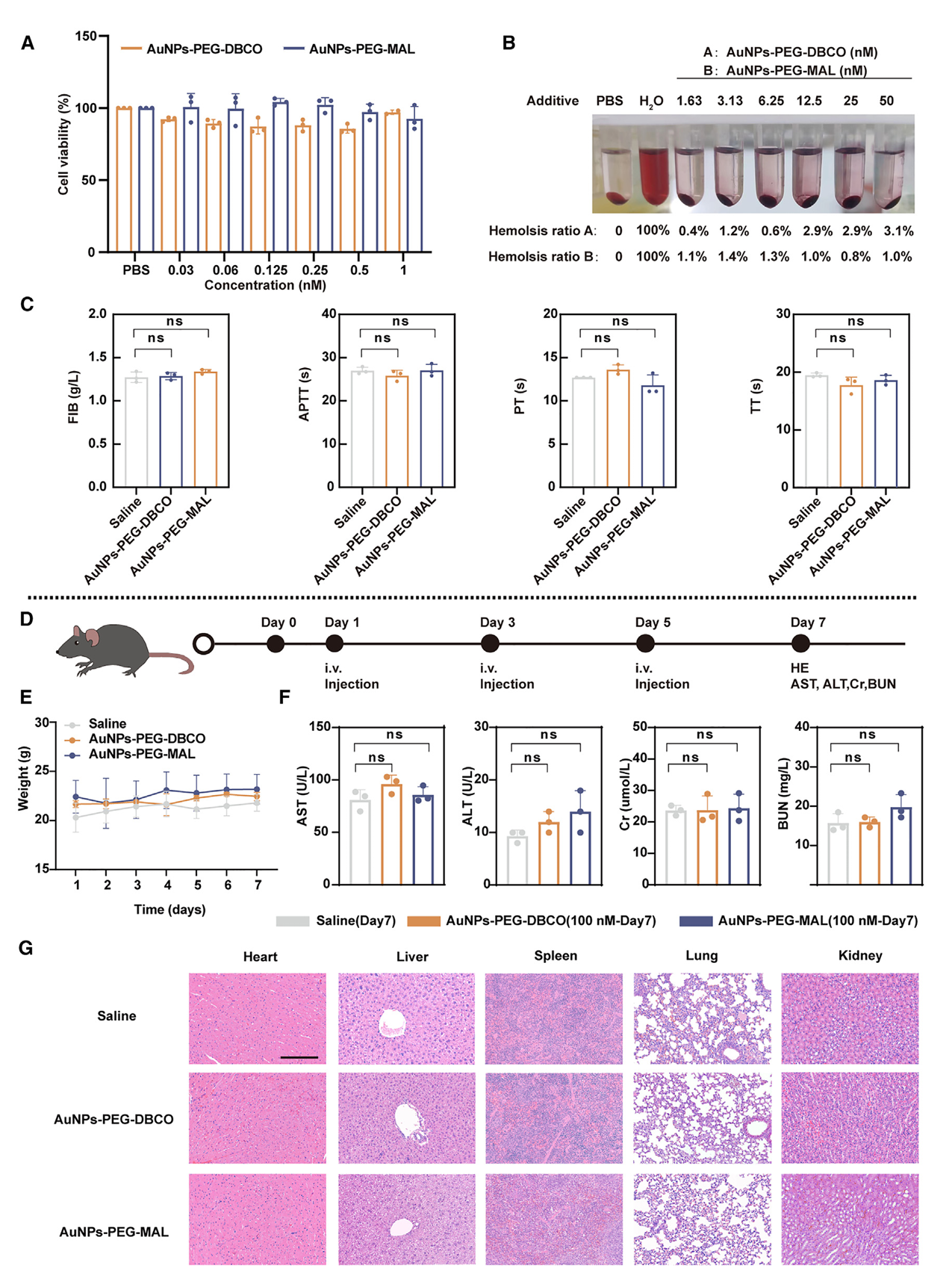
图6:AuNP-PEG-DBCO和AuNPs-PEG-MAL的生物安全性
论文链接://doi.org/10.1016/j.matt.2025.101997